氢键在物理、化学、生命科学和材料科学等自然科学中的重要性不言而喻。科学家在研究氢键的时候经常会涉及到氢键对称性的问题。在对称氢键中,质子处于两个相同的离子、分子或分子片的正中央,势能面上仅存在一个势阱(图1a;左)。对于非对称X−H···X氢键,双势阱势能面中的对称结构为过渡态(图1a;右)。图1b中给出了一些对称氢键的例子:对称N···H···N氢键存在于质子化1,6-二氮杂双环[4.4.4]十四烷(1)中;对称O···H···O氢键存在于马来酸氢盐(2)中;对称F···H···F氢键存在于氟氢化物中。考虑到C与N、O、F同周期且其电负性比H强,从理论上讲,对称C···H···C氢键也是有可能存在的。但是,文献中却鲜有关于对称C···H···C氢键的实验或理论研究。
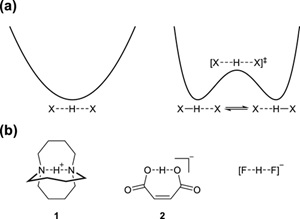
图1. (a)氢键的对称性;(b)对称氢键示例。
最近,余志祥教授和研究助理王熠博士通过理论计算首次提出了对称C···H···C氢键存在的可能性。作者首先以甲烷与甲基负离子所形成的氢键复合物为例论证了对称C···H···C氢键存在的理论基础。如图2所示,当两个碳原子之间的距离被固定为2.90 Å时,体系展现出了双势阱势能面的特征。随着两个碳原子不断靠近,势能面逐渐由双势阱向单势阱过渡。最终,当两个碳原子之间的距离被缩短至2.50 Å时,体系中首次出现了对称的碳氢碳氢键。
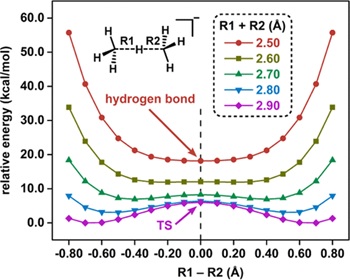
图2. 势能面扫描。
然而,在上述例子中具有对称氢键的结构并不是体系的能量极小点。因此,接下来他们开始着手于利用理论计算设计一些更加合理的对称C···H···C氢键。为了将两个碳原子之间的距离固定在2.5 Å附近,作者参考了质子化1,6-二氮杂双环[4.4.4]十四烷(1;其结构如图1b所示)中的对称N···H···N氢键。在该结构中,两个氮原子之间的距离为2.53 Å。他们试图通过设计分子内C···H···C氢键,并利用环张力强迫两个碳原子靠近(图3;左)。但是,这一策略并未取得成功。经过几何优化,作者发现体系能量极小点中的C−H···C氢键是非对称的,且两个碳原子之间的距离长达2.93 Å。为了进一步缩短两个碳原子之间的距离,作者通过引入笼状结构(例如桶烯)进一步增加了体系的环张力。如图3(右)所示,此时体系能量极小点中两个碳原子之间的距离仅为2.53 Å,且C···H···C氢键是对称的。至此,作者成功例证了对称C···H···C氢键存在的可能性。
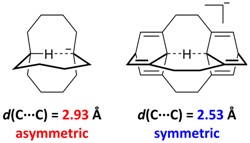
图3. 非对称C−H···C氢键(左)和对称C···H···C氢键(右)。
最后,作者对合成该碳负离子的途径进行了理论研究。如图4所示,由烃类前体11到目标碳负离子7的转化在热力学上是可行的。这意味着(至少在气相中)烃类前体11具有比水分子更强的酸性。同时,这些反应的活化能均不高(小于20 kcal/mol),这意味着目标碳负离子7有机会在较为温和的反应条件下被合成出来。基于这些正面的初步结果,作者期望合成化学家能够在不久的将来设计出更加合理的反应前体,并在实验上成功实现对称C···H···C氢键的构筑。该工作发表在J. Org. Chem. 2020, 85, 397。 以上工作在X-Mol上也有相关介绍(https://www.x-mol.com/news/158535)。
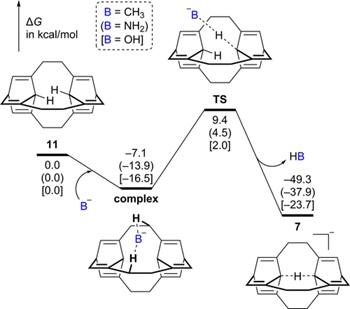
图4. 由烃类前体11转化为碳负离子7的势能面。