放疗使临床中超过50%的癌症病人获益。联合放化疗已成为肺癌、结直肠癌、胃癌等多种癌症的一线疗法。然而传统化疗药物通常具有较强的毒副作用,严重影响患者的生存质量。放疗响应药物(Radiotherapy-Activated Prodrug, RAP)是一类低毒性的前体药物,可在电离辐射作用下被特异性激活,进而释放出具有治疗活性的药物分子。其作用机制主要依赖于电离辐射引发的水辐解反应所产生的活性物种(如羟基自由基和水合电子),通过这些活性物种驱动前体药物发生特定化学转化,实现活性药物的可控释放,从而有望建立一种低毒性、高选择性的联合放化疗新策略。
近日,北京大学化学与分子工程学院应用化学系/北大-清华生命科学联合中心刘志博团队在ACS Central Science上发表了题为“Radiotherapy-Activated Prodrug: Past, Present and Beyond”的展望综述。该文章总结了放疗响应药物领域的最新进展,并从电离辐射类型,辐射响应化学机制、前体药物形式以及适应症等多个方向进行了展望,以期助力该领域的进一步发展。
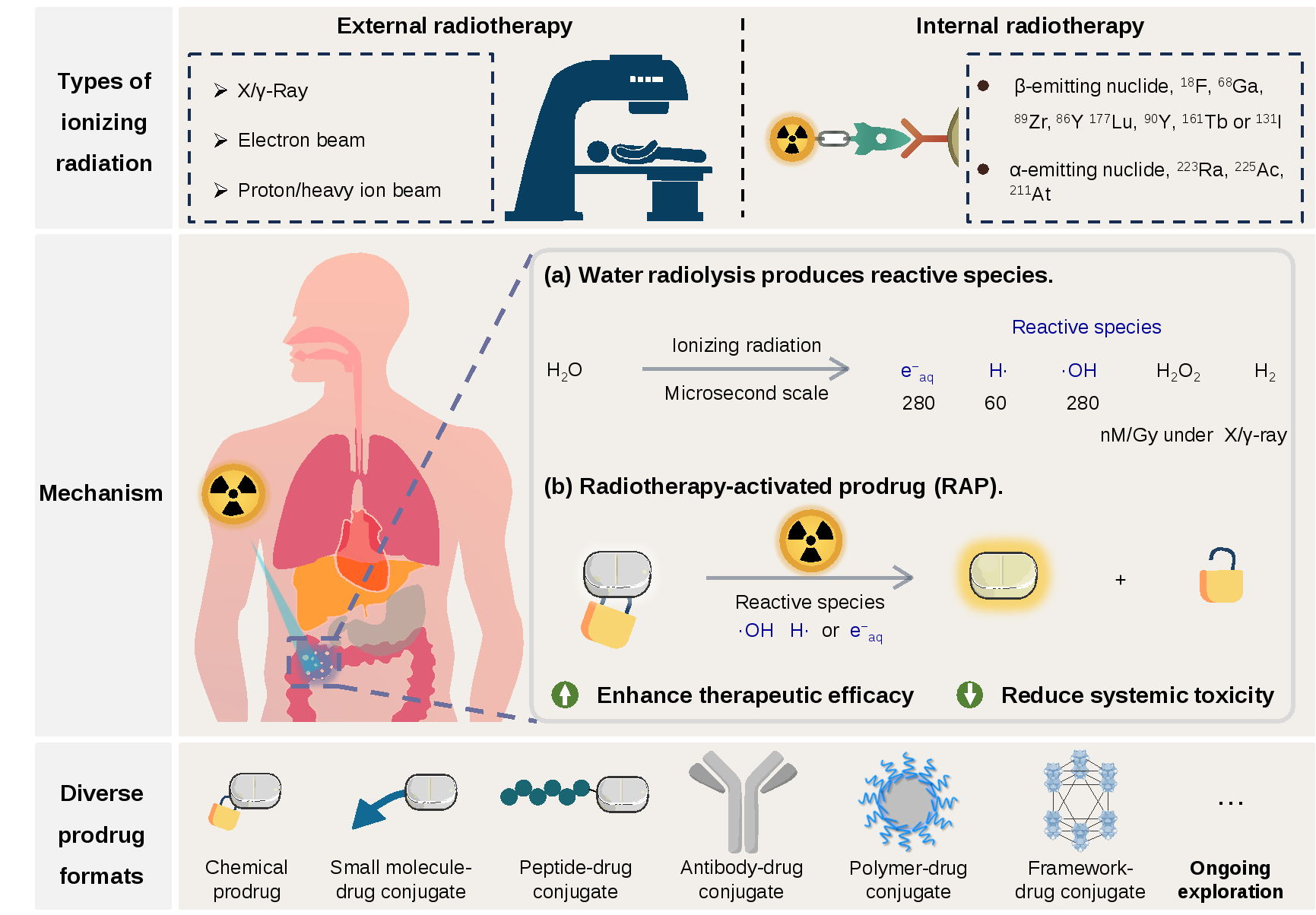
图1. 放疗响应药物的研究现状
本文首先回顾了RAP技术的发展历程,总结了该领域早期的探索。由于受到多种因素限制,前期研究最终未能取得成功。近年来,随着放疗联合治疗在临床中的应用需求不断增长,2020年刘志博团队首次报道了放疗驱动的活体内RAP技术。在此过程中,更精准的辐射递送技术、更高效的辐射响应化学结构以及更强效的药物类型相继涌现,推动了该领域的迅速发展。此外,不仅原位放疗射线可激活药物,肿瘤靶向放射性核素药物也能够在活体内介导化学转化,为转移瘤治疗提供了新策略。
RAP技术有望显著降低传统化疗引发的系统毒性,推动同步放化疗向更精准、安全及高效的方向发展,从而重塑癌症治疗的临床范式。此前,刘志博团队在Medicine Plus期刊发表了题为“Perspective to clinical translation of radiotherapy-activated prodrugs: challenges and advances”的评述文章,系统探讨了放疗激活前药在临床转化过程中面临的挑战与前沿进展。目前,该团队正稳步推进RAP技术的临床转化研究,已成功筛选出临床前候选分子,并通过多轮专家咨询与临床方案论证,进一步明确了其临床适应症方向。预计未来两年内,该候选分子将进入注册临床试验阶段,有望加速RAP技术的临床应用进程,最终造福广大肿瘤患者。
北京大学化学与分子工程学院/北大-清华生命科学联合中心/昌平实验室刘志博教授为该论文通讯作者,北京大学博雅博士后王常伦为论文第一作者。该工作得到了北京大学化学与分子工程学院、北大-清华生命科学联合中心、昌平实验室、北京分子科学国家研究中心、中华人民共和国科学技术部、国家杰出青年科学基金、北京市自然科学基金等机构和项目的资助。
放疗响应药物介绍:
https://baike.baidu.com/item/放疗响应药物/63863888
原文链接:
https://pubs.acs.org/doi/10.1021/acscentsci.5c00875
https://www.sciencedirect.com/science/article/pii/S2950347725000076
审核:牛林,杨四海