免疫治疗药物研发面临的一个重大挑战是“在靶脱瘤(on-target off-tumour, OTOT)”毒性的发生,包括强效免疫激动剂引发的致命性"细胞因子风暴"。若能将这类药物通过分子工程改造为低毒性的前药,在肿瘤部位选择性激活以诱导抗肿瘤免疫,有望降低OTOT毒性。
近期,北京大学/昌平实验室的刘志博教授团队和清华大学/昌平实验室的傅阳心教授团队合作在Nature Communications期刊“背靠背”发表了2篇研究论文,题为:1)Single Atom Engineering for Radiotherapy-Activated Immune Agonist Prodrugs和2)Orchestrating Intratumoral DC-T Cell Immunity for enhanced Tumor Control via Radiotherapy-activated TLR7/8 prodrugs in mice,分别从前药开发技术和生物学机制角度共同阐述了一种抗肿瘤免疫放疗响应药物策略。
第一篇论文基于刘志博课题组的放疗响应药物技术(Radiotherapy-Activated Prodrug, RAP),针对小分子免疫激动剂IMDQ类分子存在的OTOT毒性问题与靶向递送需求,开发了单原子工程化的放疗响应的免疫激动剂前药(O-IMDQ),通过计算机辅助的药物设计,利用单个氧原子的化学修饰给IMDQ的活性“上锁”,其活性(EC50值)可被抑制4000倍以上,使其在进入体内后处于“沉默”状态。此后,在肿瘤内通过放疗照射“解锁”恢复药物活性,诱导抗肿瘤免疫使肿瘤消退,甚至激活放疗的“远端效应”。
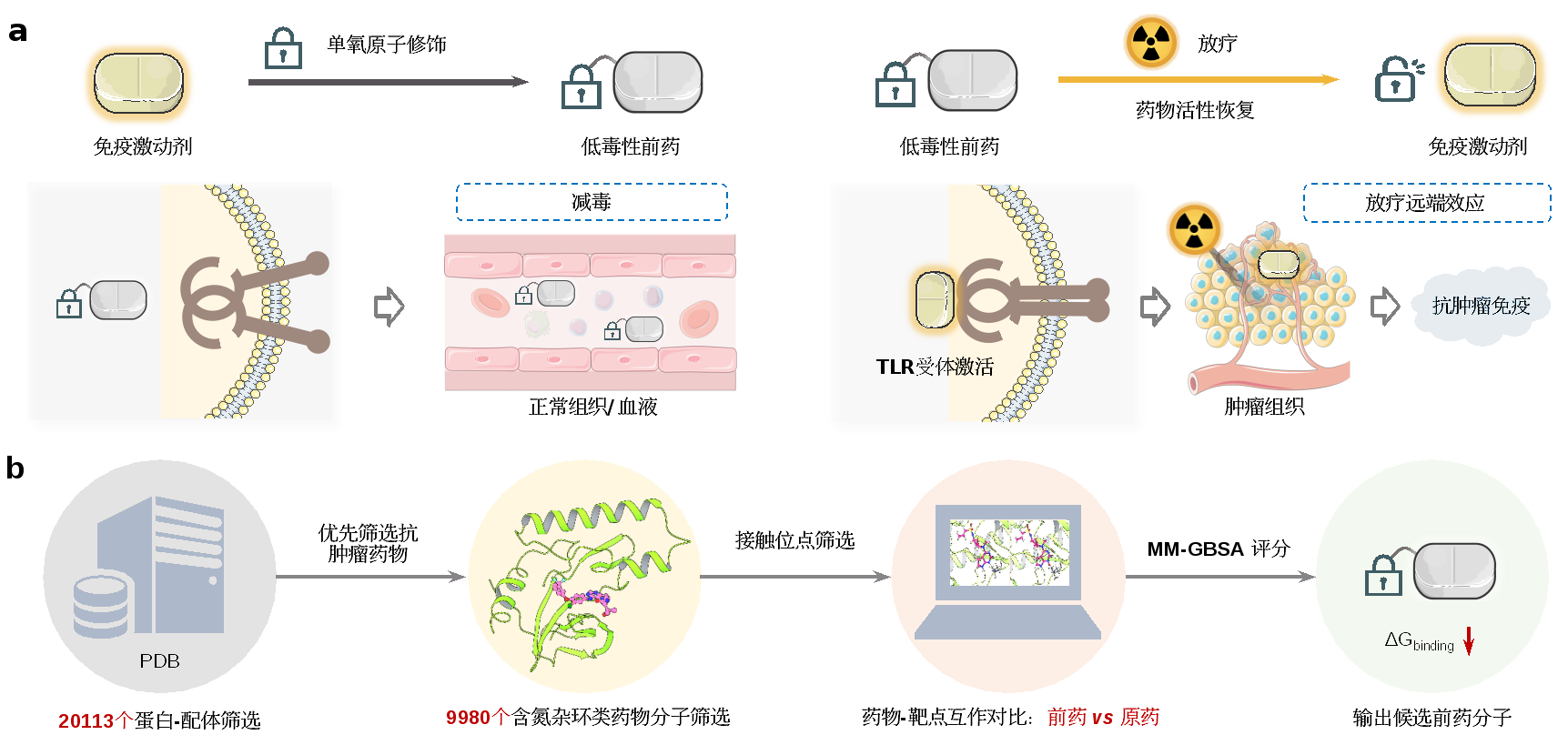
图1. 利用单个氧原子可抑制免疫激动剂毒性,并可通过放疗实现肿瘤靶向的重新激活。
第二篇论文重点解析放疗响应免疫激动剂前药的抗肿瘤免疫机制。在此项工作中,傅阳心教授团队利用刘志博教授团队开发的RAP技术与O-IMDQ前药分子,探究肿瘤局部的激活作用机制。研究显示,放疗激活后产生的IMDQ激动剂能够依靠肿瘤内部既有T细胞的重新赋能,这一发现进一步强调了局部免疫激活的核心地位。进一步机制研究揭示,STING和MyD88信号通路协同调控了I型干扰素的产生,从而驱动DC介导的T细胞激活,形成以肿瘤微环境为中心的免疫循环。
综上,两项研究以RAP技术开发为起点、以免疫激活的机制为应用场景和目标科学问题,探索了放疗引导下局部免疫“点火”机制,成功构建出兼具疗效与安全的新型抗肿瘤策略。此外,该平台技术可针对其他多种靶点开发高原子经济性(仅单个氧原子修饰)的放疗响应药物,为临床放射联合化疗/免疫治疗提供了新对策。
两项研究的通讯作者是北京大学化学与分子工程学院的刘志博教授和清华大学医学院的傅阳心教授。昌平实验室副研究员丁泽轩博士、清华大学尹晓哲博士、北京大学化学与分子工程学院博士生郑越丹、北大-清华生命联合中心博士生李奕言为第一篇文章开发单原子工程化RAP平台技术的共同第一作者,尹晓哲博士、丁泽轩博士、清华大学余莉博士为第二篇文章探索抗肿瘤免疫机制的共同第一作者。该工作得到了北京大学化学与分子工程学院、北大-清华生命科学联合中心、昌平实验室、北京分子科学国家研究中心、中华人民共和国科学技术部、国家杰出青年科学基金、北京市自然科学基金等机构和项目的资助。
论文链接:
1)前药技术开发 https://doi.org/10.1038/s41467-025-60768-4
2)肿瘤免疫机制 https://doi.org/10.1038/s41467-025-60769-3
审核:牛林,杨四海